1.Cuanto
En este último bimestre del curso de "temas de Física" se está abarcando en su gran mayoría temas englobados en la física moderna, entre los que podemos encontrar:
- cuantos
- teoría de la relatividad
- predicibilidad
- caos
- núcleo
- radiactividad
- fusión
- fisión
A continuación se describirán cada uno de los puntos anteriormente mencionados. Cabe recalcar que la "física moderna" NO es difícil de entender. siempre y cuando pongamos dedicación, empeño e interés. Espero y les sea de ayuda esta información ....
En física, el término cuanto o cuantio (del latín Quantum, plural Quanta, que representa una cantidad de algo) denotaba en la física cuántica primitiva tanto el valor mínimo que puede tomar una determinada magnitud en un sistema físico, como la mínima variación posible de este parámetro al pasar de un estado discreto a otro. Se hablaba de que una determinada magnitud estaba cuantizada según el valor de cuanto. Es decir, cuanto es una proporción hecha por la magnitud dada.
Un ejemplo del modo en que algunas cantidades relevantes de un sistema físico están cuantizadas se encuentra en el caso de la carga eléctrica de un cuerpo, que sólo puede tomar un valor que sea un múltiplo entero de la carga del electrón. En la moderna teoría cuántica aunque se sigue hablando de cuantización el término cuanto ha caído en desuso. El hecho de que las magnitudes estén cuantizadas se considera ahora un hecho secundario y menos definitorio de las caracterísitcas esenciales de la teoría.
En informática, un cuanto de tiempo es un pequeño intervalo de tiempo que se asigna a un proceso para que ejecute sus instrucciones. El cuanto es determinado por el planificador de procesos utilizando algún algoritmo de planificación.
EXPLICACIÓN CIENTÍFICA DEL CONCEPTO DEL CUANTO DE ENERGÍA: Durante más de dos siglos la física newtoniana resultó válida para describir todos los fenómenos concernientes a materia y energía. Después, en el siglo XIX, la teoría electromagnética reveló que la energía podía existir con cierta independencia de la materia, en forma de radiaciones de muy diferentes longitudes de onda y frecuencias. Al mismo tiempo, el estudio de la termodinámica abordó problemas suscitados por la energía calorífica y su distribución en sistemas como los gases, cuyas partículas resultaban demasiado pequeñas para ser medidas u observadas.
 Era imposible —y afortunadamente innecesario— predecir el comportamiento de cada molécula o de cada átomo, pero las leyes estadísticas de la probabilidad podían aplicarse a grandes conjuntos de partículas, dentro de una reducida muestra o sistema.
Era imposible —y afortunadamente innecesario— predecir el comportamiento de cada molécula o de cada átomo, pero las leyes estadísticas de la probabilidad podían aplicarse a grandes conjuntos de partículas, dentro de una reducida muestra o sistema.
En un gas, a determinada temperatura, unas moléculas se mueven muy lentamente y otras con gran celeridad: sin embargo, la energía media de todas las moléculas en movimiento depende exclusivamente de la temperatura y de la presión a que dicho gas esté sometido si el volumen es constante. Max Planck (a la izquierda) fue uno de los muchos científicos que trataron de aplicar los principios de la termodinámica a las radiaciones. Él, científico alemán (1858-1947) fue el responsable de introducir una innovación que cambiaría para siempre el rumbo de la Física.
Probando distintas funciones y haciendo infinidad de cálculos, Planck había encontrado (sin deducirla de principios de la Física) una fórmula que describía muy bien los espectros experimentales de los cuerpos negros.
Pero encontrar la forma funcional de una relación no significa explicar por qué resulta así. Esta fórmula se resistía a ser deducida de los principios clásicos. Entonces Planck, sin demasiado convencimiento, se vio obligado a introducir un postulado que no tenía, en principio, ninguna justificación, pero que le permitía predecir perfectamente los espectros de radiación que la naturaleza mostraba. Era el siguiente:
"Los osciladores microscópicos responsables de la emisión electromagnética no pueden emitir o absorber cualquier valor de energía. Si el oscilador tiene frecuencia y, sólo emitirá o absorberá múltiplos enteros del cuanto de energía E = h . v (donde h es la constante de Planck).
El valor de h es muy pequeño, 6,63. 1O–34 J . s, y resultó ser una constante universal, fundamental dentro de la teoría cuántica."
Comportamiento encontrado por Planck para la emisión de un cuerpo negro P(µ,T) es la potencia
emitida y µ es la longitud de onda
emitida y µ es la longitud de onda
Para fines del siglo XIX, se sabía que la radiación de un cuerpo negro se debía a las oscilaciones de las partículas cargadas de la superficie de estos cuerpos. Sin embargo, a partir del electromagnetismo clásico era imposible deducir los espectros y las leyes experimentales de Stefan-Boltzmann y de Wien. La Física clásica había llegado a un límite que no podría superar.
Que la energía estuviera cuantízada, que no fuera continua sino discreta, era tan absurdo como suponer que cuando una piedra cae libremente no puede pasar por todas las alturas posibles, sino que va saltando, de una posición a otra mas distante sin pasar por las intermedias.
En un principio este resultado no causó gran conmoción en la comunidad científica, pues se lo consideró como un artilugio con poco asidero real.
Según la teoría clásica de las ondas electromagnéticas, éstas transportan energía en forma continua y no en paquetes discretos o cuantos. Vemos que la luz de una vela llena una habitación con un flujo constante de energía. Sin embargo, la cuantización implicaría una emisión espasmódica de la luz, como si la vela parpadeara, encendiéndose y apagándose intermitentemente (que es en realidad lo que ocurre en el nivel microscópico!). El mismo Planck no podía creer que esto fuera así. Pasarían algunos años hasta que el cuanto de energía fuera aceptado como una realidad.
Calculemos el valor del cuanto de energía para una onda electromagnética de la región visible de frecuencia 5. 1O14 Hz (amarillo):
E = h . v 6,63. 1O–34 J. s . 5. 1014 Hz = 3,3. 10–19 J.
Este valor de energía es diminuto. La energía que libera una pequeña luciérnaga, por ejemplo, contiene miles de millones de cuantos. Esto hace que la cuantización de la energía de las ondas electromagnéticas no tenga efectos macroscópicos, pero sí tiene peso cuando se estudian fenómenos a escala atómica.
HACIA LA MECÁNICA CUÁNTICA
Estas ideas de Planck y Bohr se van a difundir, a ampliar y después a revolucionar con la llegada de una nueva Mecánica, la Mecánica Cuántica, que deriva directamente de ellas. Gracias a esta revolución conceptual se va a tener que renunciar a cualquier descripción determinista de la realidad para acogerse a una descripción en términos de probabilidad.
Estas ideas de Planck y Bohr se van a difundir, a ampliar y después a revolucionar con la llegada de una nueva Mecánica, la Mecánica Cuántica, que deriva directamente de ellas. Gracias a esta revolución conceptual se va a tener que renunciar a cualquier descripción determinista de la realidad para acogerse a una descripción en términos de probabilidad.
Así es como se llegó a la conclusión de que no se puede conocer al mismo tiempo la posición y la velocidad de una partícula. Se va a demostrar también que cualquier medida perturba el fenómeno que quiere estudiar. Es el famoso principio de incertidumbre deHeisenberg.
En resumidas cuentas, con la Mecánica cuántica se entra en un nuevo mundo palpitante, misterioso y extraño que se ha explorado sobre bases matemáticas sólidas entre los años 1925-1930, bajo el impulso de sabios cuyos nombres son ya legendarios, como el austríaco Erwin Schródinger, el alemán Werner Heisenberg, el suizoalemán Wolfgang Pauli, el inglés de Cambridge Paul Dirac, todo bajo el impulso constante de Niels Bohr, y a pesar del escepticismo de Albert Einstein. Pero ésa es otra historia, casi una epopeya.
Einstein había visto antes que nadie todas las implicaciones de la Mecánica cuántica. Pero por razones filosóficas, y casi teológicas, no podía aceptarla. Es el famoso ¡«Dios no juega a los dados»!
Sobre lo que nosotros queremos insistir aquí es que muchos fenómenos pueden quedar sencillamente explicados —o al menos claramente expuestos— partiendo del átomo de Bohr ligeramente modificado. No cabe duda de que se trata de una primera aproximación, que no corresponde a la realidad tal como la concebimos hoy en día, pero tiene la ventaja de evitar el despliegue matemático y la complejidad intelectual inherentes a la Mecánica cuántica (que, si se quiere captar su espíritu, necesita larguísimos cálculos, ya que el mundo de lo infinitamente pequeño obedece a reglas específicas muy diferentes de las que gobiernan nuestra experiencia cotidiana).
LOS NIVELES DE ENERGÍA
En cada átomo, en cada molécula, existen niveles de energía en los que pueden «situarse» los electrones. Esos niveles se corresponden con los cuanta y por lo tanto están, como hemos dicho, separados por intervalos vacíos, lo mismo que los peldaños de una escalera. Los electrones no pueden hallarse más que en esos niveles, lo mismo que nuestros pies no se pueden colocar más que en los peldaños de la escalera.
En cada átomo, en cada molécula, existen niveles de energía en los que pueden «situarse» los electrones. Esos niveles se corresponden con los cuanta y por lo tanto están, como hemos dicho, separados por intervalos vacíos, lo mismo que los peldaños de una escalera. Los electrones no pueden hallarse más que en esos niveles, lo mismo que nuestros pies no se pueden colocar más que en los peldaños de la escalera.
Naturalmente, esto es la representación del átomo bajo el punto de vista de la energía. Bajo el punto de vista del espacio, el electrón se mueve sin cesar, gira en torno al núcleo, pero en una órbita impuesta por los niveles de energía autorizados.
Esos niveles de energía no pueden «contener» más que un número finito de electrones. Por ejemplo, el primer nivel de energía de un átomo, el primer peldaño, no puede llevar más que dos electrones, el segundo es un peldaño doble que, en total, no puede contener más que 8 electrones (2 + 6), etcétera.
¿Cómo puede situarse un electrón en esta escalera?
Se llenan los peldaños comenzando por abajo, según el principio de energía mínima, pasando poco a poco de uno a otro. Así es como, en cada átomo estable, hay niveles de energía llenos. El último nivel lo está más o menos completamente.
Se llenan los peldaños comenzando por abajo, según el principio de energía mínima, pasando poco a poco de uno a otro. Así es como, en cada átomo estable, hay niveles de energía llenos. El último nivel lo está más o menos completamente.
Pero por encima del último nivel lleno hay otros niveles (otros peldaños de la escalera) totalmente vacíos. A estos niveles se les llama niveles «excitados».
¿Puede un electrón abandonar un nivel de energía que ocupa normalmente (y que se llama el nivel estable) para pasar a un nivel de energía excitado? Pues sí, pero para eso hay que proporcionarle la energía suficiente para que logre saltar de un nivel a otro. Pero cuidado, es menester que la energía que se le comunica sea exactamente la que corresponde a la diferencia de energía que existe entre los dos peldaños, lo que se llama el «cuantum» justo de energía.
¿Y esos electrones excitados situados en órbitas libres van a permanecer allí?
Respuesta: sí, pero no por mucho tiempo. Los niveles de excitación no son los niveles de equilibrio para los electrones. Así pues, éstos van a tener tendencia a caer los niveles de energía habituales (hogar, dulce hogar) y, por lo tanto, a volver a ellos.
Respuesta: sí, pero no por mucho tiempo. Los niveles de excitación no son los niveles de equilibrio para los electrones. Así pues, éstos van a tener tendencia a caer los niveles de energía habituales (hogar, dulce hogar) y, por lo tanto, a volver a ellos.
Cuando lo hacen, la energía tiene que conservarse. La caída de un electrón de un nivel elevado hacia uno más bajo va a ir acompañada de una liberación de energía, por ejemplo mediante la emisión de una luz cuya longitud de onda (el color) será exactamente igual a la de la luz que ha excitado el átomo.
2.Teoría de la relatividad
Para continuar el homenaje a Albert Einstein, vamos a repasar ahora brevemente la Relatividad General en un texto que sirve como introducción para aquellos no iniciados en esta rama de la física. La teoría general de la relatividad de Albert Einstein es uno de los logros más imponentes de la física del siglo veinte. Publicada en 1916, explica lo que percibimos como «fuerza de gravedad». De hecho, esta fuerza surge de la curvatura del espacio y del tiempo. Einstein propuso que los objetos como el Sol y la Tierra variaban la geometría del espacio.
En presencia de materia y energía, el espacio se puede deformar y estirar, formando cordilleras, montañas y valles que causan que los cuerpos se muevan por estas "rutas" curvas.
DURANTE más de dos siglos, la mecánica de Newton dominó completamente en la física: el Universo entero parecía comportarse tal como lo predecían las ecuaciones de la física newtoniana y la comprensión de la naturaleza se había reducido a un problema de técnica matemática. Pero a principios del siglo XX empezaron a surgir evidencias de que la física clásica, así como todos los conceptos relacionados con ella, no describe adecuadamente a los fenómenos que suceden a la escala de los átomos o a velocidades comparables a la de la luz.
La mecánica clásica constituye una excelente aproximación a la realidad, dentro de ciertos límites.
Sin embargo en la escala microscópica, los fenómenos físicos sólo pueden estudiarse por medio de la mecánica cuántica. Y cuando se tratan velocidades muy altas, cercanas a la luminosa, se debe recurrir a la teoría de la relatividad. La primera revolución científica del siglo XX se produjo cuando Albert Einsteinformuló, en 1905, la teoría de la relatividad especial.
A continuación describiremos los rasgos esenciales de esta teoría.
Para estudiar o describir un fenómeno físico debemos recurrir necesariamente a un «sistema dereferencia» con respecto al cual efectuamos mediciones. En la práctica cotidiana el sistema de referencia que más se utiliza, es la Tierra misma que, en general, se supone inmóvil, a pesar de que gira sobre sí misma y alrededor del Sol, recorriendo el espacio cósmico a una velocidad de 30 km/seg.
En cambio, para describir el movimiento de los planetas, es más conveniente utilizar al Sol como punto de referencia, o, más precisamente, como centro de un sistema de referencia donde este astro está fijo. Pero ni el Sol, ni las estrellas vecinas a él, se encuentran realmente fijos: el Sol se halla en las regiones externas de una galaxia que rota dando una vuelta completa en millones de años. A su vez, esta galaxia se mueve con respecto a otras galaxias, etcétera.
En la práctica afortunadamente, no es necesario tomar en cuenta todos estos movimientos porque las leyes de la física son las mismas en cualquier sistema de referencia. Este principio fundamental se aplica aun para sistemas de referencia terrestres: en la época de Galileo, los filósofos discutían si una piedra, lanzada desde lo alto del mástil de un barco en movimiento, cae verticalmente con respecto al barco o con respecto a la Tierra.
Así, todo movimiento es relativo al sistema de referencia en el cual se observa y, las leyes de la física, no cambian de un sistema a otro. Este hecho fundamental se conoce como principio de relatividad de Galileo.
Sin embargo, los filósofos y los físicos clásicos veían con desagrado —quizá con vértigo— el hecho de que no existiera un sistema de referencia absoluto con respecto al cual definir todos los movimientos del Universo. Estrictamente hablando, el principio de relatividad no excluye la existencia de tal sistema absoluto, únicamente postula que las leyes de la física son las mismas en ese y en cualquier otro sistema.
Pero, a mediados del siglo XIX, surgieron las primeras dificultades de la relatividad galileana, cuando el físico escocés James Clerk Maxwell formuló la teoría matemática de los fenómenos eléctricos y magnéticos.Maxwell demostró que la electricidad y el magnetismo son dos aspectos de un mismo fenómeno: el electromagnetismo. Como una de las consecuencias más importantes de su teoría descubrió que la luz es una vibración electromagnética que se propaga exactamente como una onda.
Pero las ondas lo hacen en medios materiales, por lo que los físicos del siglo pasado postularon la existencia de un medio extremadamente sutil, el éter, que llenaba al Universo entero, permeaba todos los cuerpos y servía de sustento a la luz. Según esta concepción, la luz sería una vibración del éter del mismo modo que el sonido es una vibración del aire.
De existir el éter, sería un sistema de referencia absoluto con respecto al cual medir el movimiento de todos los cuerpos en el Universo. Más aún, se descubrió que las ecuaciones de Maxwell cambian de forma al pasar de un sistema de referencia a otro, lo cual implicaría que el principio de relatividad no se aplica a los fenómenos electromagnéticos.
Se postuló, entonces, que estas ecuaciones sólo son válidas en el sistema de referencia del éter en reposo. Esto no es sorprendente pues la luz, fenómeno electromagnético, se propaga con una velocidad bien definida en el éter y esta velocidad debe ser distinta en un sistema de referencia en movimiento con respecto al éter.
Al parecer, la teoría electromagnética de Maxwell restituía un sistema de referencia absoluto.
La manera más evidente de confirmar las ideas anteriores es medir la velocidad de la luz, emitida en direcciones opuestas, en la Tierra:
la diferencia de velocidades puede llegar a ser tan grande como 60 km/seg .
Esta velocidad es muy pequeña con respecto a la velocidad total de la luz, que es de 300 000 km/seg, pero, a fines del siglo pasado, los físicos experimentales Michelson y Morley lograron construir un aparato que permitía medir diferencias aún más pequeñas en la velocidad de un rayo luminoso.
Michelson y Morley realizaron su experimento en 1887: para sorpresa de la comunidad científica de esa época, no detectaron ningún cambio de la velocidad de la luz. Esta velocidad era la misma en cualquier dirección, independientemente de cómo la Tierra se mueva con respecto al hipotético éter.
Para empezar, Einstein postuló que las ecuaciones de Maxwell del electromagnetismo son rigurosamente válidas en cualquier sistema de referencia. Esta condición de invariancia se cumple a condición de que el tiempo medido en un sistema no coincida con el medido en otro sistema.
Este hecho no había sido tomado en cuenta por los antecesores de Einstein y, por esta razón, las ecuaciones de Maxwell parecían violar el principio de relatividad.
Habiendo postulado que no puede haber ningún sistema de referencia privilegiado, Einstein concluyó que el éter simplemente no existe. Pero, entonces ¿con respecto a qué debe medirse la velocidad de la luz? La respuesta de Einstein fue drástica:
«la velocidad de la luz es la misma en cualquier sistema de referencia».
Después de todo, eso es lo que indica el experimento de Michelson y Morley.
Este concepto de la invariancia de la velocidad de la luz contradice nuestro "sentido común". Si lavelocidad de la luz es de 300 000 km/seg, esperaríamos que al perseguir una señal luminosa veamos que se mueve con una velocidad menor. (Si, por ejemplo, corremos a 80 km/hora detrás de un tren que se mueve a 100 km/hora, vemos que el tren se mueve con respecto a nosotros a 20 km/hora.)
Sin embargo, debido a la no invariancia del tiempo, las velocidades no se adicionan o sustraen en el caso de señales luminosas (o, en general, de partículas que se mueven casi tan rápidamente como la luz).
Los efectos predichos por la teoría de la relatividad son imperceptibles en nuestra vida cotidiana y sólo se manifiestan cuando se involucran velocidades comparables a la de la luz.
Consideremos, como ejemplo, una nave espacial que se mueve con una velocidad muy alta: despegade la Tierra y regresa después de recorrer cierta distancia.
Según la relatividad, el tiempo transcurre normalmente tanto para los que se quedaron en la Tierra como para los pasajeros de la nave, pero esos dos tiempos no son iguales.
Al regresar a la Tierra, los tripulantes de la nave constatarán que el viaje duró para ellos un tiempo menor que para los que se quedaron.
Más precisamente, el tiempo medido en la nave es más pequeño que el medido en la Tierra por un factor de acortamiento
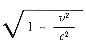
donde v es la velocidad de la nave y c la velocidad de la luz.
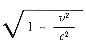
donde v es la velocidad de la nave y c la velocidad de la luz.
Para velocidades v del orden de algunos metros o kilómetros por segundo, como las que ocurren comúnmente en nuestras experiencias diarias, el factor de acortamiento es tan cercano al valor 1 que es imposible detectar el efecto relativista del cambio de tiempo. Si la nave espacial viaja a unos 10 000 km/hora, la diferencia entre los tiempos medidos será apenas una diez millonésima de segundo por cada hora transcurrida (lo cual, incidentalmente, se ha podido confirmar con la tecnología moderna).
Pero, en el otro extremo, si la nave viaja a una velocidad muy cercana a la de la luz, su tiempo puede ser muy corto con respecto al transcurrido en la Tierra: por ejemplo, a la velocidad de 295 000 km/seg, una nave espacial tardaría unos 20 años medidos en la Tierra para ir a la estrella Sirio y regresar; sin embargo, para los tripulantes de la nave habrán pasado ¡sólo 3 años y medio!
La contracción del tiempo no es el único efecto sorprendente que predice la teoría de la relatividad. Einstein también demostró que existe una equivalencia entre la energía y la masa, dada por la famosa fórmula
E= mc2
donde E es la energía equivalente a una masa m de materia.
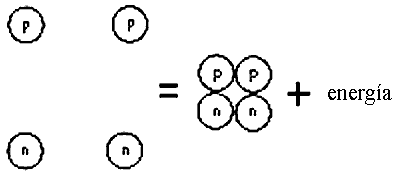
Por ejemplo, el núcleo de un átomo de helio está constituido por dos protones y dos neutrones, pero la masa del núcleo de helio es un poco menor, cerca del 4%, que la masa sumada de dos protones y dos neutrones separados (Figura a); en consecuencia, al unirse estas cuatro partículas pierden una fracción de masa que se transforma en energía; éste es el principio de la fusión nuclear, que permite brillar al Sol y a todas las estrellas (y construir bombas atómicas).
Un núcleo de helio pesa menos que sus componentes por separado:
dos protones y dos neutrones.
Al formarse un núcleo de helio, la diferencia de masa se libera
en forma de energía (fusión nuclear).
De la fórmula E = mc² no se deduce que cualquier masa se puede transformar en energía o viceversa; este proceso se da sólo en condiciones muy particulares. Hemos mencionado la fusión nuclear, pero la manera más eficiente de transformar masa en energía es por la aniquilación
de la materia con la antimateria.
Al entrar en contacto una partícula con su correspondiente antipartícula, las dos se aniquilan
totalmente quedando sólo energía en forma de rayos gamma:
la eficiencia de este proceso de transformación de materia en energía es del 100%.
Para aumentar la velocidad de un cuerpo, hay que proporcionarle energía, lo cual se manifiesta como un aumento de la masa del cuerpo. La teoría de la relatividad predice
que la energía necesaria para que un cuerpo de masa m alcance la velocidad v es
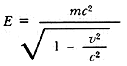
En el límite v = 0, se recupera la fórmula E = mc² para la energía ya existente en forma de masa.
En el otro extremo, la energía E aumenta con la velocidad (Figura b) y se necesita una energía infinita para que el cuerpo alcance la velocidad de la luz.
Es por ello que, según la teoría de la relatividad, ningún cuerpo puede alcanzar o superar la velocidad de la luz. La excepción es la luz misma: según la física moderna la
luz está constituida por unas partículas llamadas fotones, la masa de
un fotón es nula y, por ello, puede viajar a la velocidad límite c.
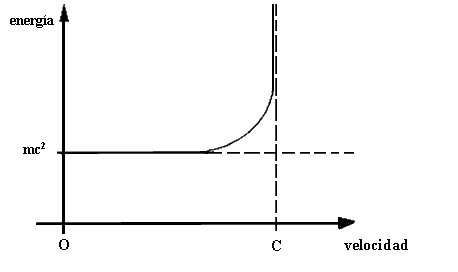
La energía de un cuerpo en movimiento aumenta con su velocidad.
Así, según la teoría de la relatividad, la velocidad de la luz es una barrera fundamental de la naturaleza que no puede ser superada. Se ha especulado sobre la existencia de posibles partículas que se mueven más rápidamente que la luz, los hipotéticos taquiones, pero nunca se ha encontrado alguna evidencia de que sean reales; más aún, de existir, se producirían situaciones contradictorias, como por ejemplo, poder regresar en el tiempo.
2.2 PREDECIBILIDAD
El término predicción puede referirse tanto a la «acción y al efecto de predecir» como a «las palabras que manifiestan aquello que se predice»; en este sentido, predecir algo es «anunciar por revelación, ciencia o conjetura algo que ha de suceder»
La predicción constituye una de las esencias claves de la ciencia, de una teoría científica o de un modelo científico. Así, el éxito se mide por el éxito o acierto que tengan sus predicciones.
La predicción en el contexto científico es una declaración precisa de lo que ocurrirá en determinadas condiciones especificadas. Se puede expresar a través del silogismo: "Si A es cierto, entonces B también será cierto."
El método científico concluye con la prueba de afirmaciones que son consecuencias lógicas del corpus de las teorías científicas. Generalmente esto se hace a través de experimentos que deben poder repetirse o mediante estudios observacionales rigurosos.
Una teoría científica cuyas aseveraciones no son corroboradas por las observaciones, por las pruebas o por experimentos probablemente será rechazada. El falsacionismo de Karl Popper considera que todas las teorías deben ser puestas en cuestión para comprobar su rigor.
Las teorías que generan muchas predicciones que resultan de gran valor (tanto por su interés científico como por sus aplicaciones) se confirman o se falsean fácilmente y, en muchos campos científicos, las más deseables son aquéllas que, con número bajo de principios básicos, predicen un gran número de sucesos.
Dificultad de predicción en numerosos campos de la ciencia:
Algunos campos de la ciencia tienen gran dificultad de predicción y pronóstico exacto. En algunos campos la complejidad de datos lo hace difícil (pandemias, demografía, la dinámica de la población, la predicción del clima, la predicción de los desastres naturales y, en general, la meteorología).
La dificultades de predicción obedece a diferentes causas:
- Variables ocultas no conocidas, en ocasiones en un proceso natural intervienen junto con ciertos factores relevantes bien identificables, medibles y cuantificables, otros factores cuya presencia o ausencia es difícil de determinar y cuya presencia tiene una influencia determinante en el resutlado de proceso. Estos factores cuya presencia es difícil o imposible de determinar es lo que se denomina "variable oculta". Las modelos de variables ocultas han sido ampliamente investigados en mecánica cuántica con el fin de construir teorías deterministas que dieran cuenta del resultado aparentemente aleatorio de ciertas medidas.
- Dinámica desconocida o compleja, en ocasiones aunque se conocen todas las variables relevantes para predecir el resultado de un proceso, las relaciones entre estas variables no se conoce con precisión, o cuando éstas se conocen las predicciones basadas en ellas son complicadas por problemas relacionados con la computación o cálculo del efecto previsible de las mismas. En concreto los sistemas con sensiblemente dependientes de las condiciones iniciales, cualquier imprecisión en la determinación de inicial de las variables hará que el valor predicho diverja con el tiempo del valor real. Dado que el sistema atmosférico mundial presenta dependencia sensible de las condiciones iniciales, la predicción del tiempo meteorológico sólo es posible con unos pocos días de antelación.
Las anteriores explicaciones son compatibles con el determinismo, una posibilidad más radical que impediría la predicción efectiva es que un fenómeno fuera efectivamente aleatorio o su comportamiento con el conocimiento actual no pudiera distinguirse del comportamiento genuinamente aleatorio.
2.3 LA TEORÍA DEL CAOS:
DEFINICIÓN Y EJEMPLO
La Teoría del Caos plantea que el mundo no sigue un patrón fijo y previsible, sino que se comporta de manera caótica y que sus procesos y comportamiento dependen, en gran manera, de circunstancias inciertas. Esto plantea que una pequeña variación en el sistema o en un punto del mismo puede provocar que en un lapso de tiempo a futuro éste presente un comportamiento completamente diferente e impredecible. No es propiamente una teoría, sino un gran campo de investigación abierto que abarca numerosas líneas de pensamiento.
De acuerdo a su definición, los sistemas dinámicos se clasifican básicamente en 3 tipos:
- Estables
- Inestables
- Caóticos
- Los sistemas estables tienden a un punto a lo largo del tiempo o siguen una misma órbita, sus ecuaciones características, condiciones iniciales, sus límites, elementos y relaciones nos permiten conocer su evolución a través del tiempo, es decir, sabemos hacia donde lo dirige su atractor.
- Los sistemas inestables, en cambio, no se guían por atractores, se escapan de éstos y no tienden hacia un punto.
- En los sistemas caóticos de pueden conocer sus ecuaciones y sus condiciones iniciales fijas, sin embargo la mas mínima variación provoca una evolución radical en su comportamiento.
- Un sistema debe presentar las siguientes propiedades para ser considerado caótico:
- Sensibilidad a las condiciones iniciales
- Debe ser transitivo
- Sus órbitas periódicas deben formar un conjunto denso en una región compacta del espacio fisico.
EL EFECTO MARIPOSA
El “efecto mariposa” es un concepto que hace referencia a la noción del tiempo a las condiciones iniciales dentro del marco de la teoría del caos. La idea es que, dadas unas condiciones iniciales de un determinado sistema caótico, la más mínima variación en ellas puede provocar que el sistema evolucione en formas completamente diferentes. Sucediendo así que, una pequeña perturbación inicial, mediante un proceso de amplificación, podrá generar un efecto considerablemente grande a mediano o corto plazo de tiempo.
Un ejemplo claro sobre el efecto mariposa es soltar una pelota justo sobre la arista del tejado de una casa varias veces; pequeñas desviaciones en la posición inicial pueden hacer que la pelota caiga por uno de los lados del tejado o por el otro, conduciendo a trayectorias de caída y posiciones de reposo final completamente diferentes. Cambios minúsculos que conducen a resultados totalmente divergentes.
Su nombre proviene de las frases: “el aleteo de las alas de una mariposa se puede sentir al otro lado del mundo” (proverbio chino) o “el aleteo de las alas de una mariposa pueden provocar un Tsunami al otro lado del mundo” así como también “El simple aleteo de una mariposa puede cambiar el mundo”.
3 El núcleo atómico |
Los primeros conocimientos sobre el núcleo atómico se los debemos a Ernest Rutherford que propuso el primer modelo atómico nuclear en 1911.
Experimento de Rutherford:
El experimento consistía en bombardear una fina lámina de oro con partículas alfa. Para observar el resultado de dicho bombardeo, alrededor de la lámina de oro colocó una pantalla fluorescente.
Estudiando los impactos sobre la pantalla fluorescente observó que:
| |
la mayoría de las partículas alfa atravesaban la lámina sin sufrir desviación;
| |
algunas se desviaban;
| |
y muy pocas rebotaban.
| |
Y lo explica del siguiente modo:
 |
La mayoría de las partículas alfa atravesaba la lámina sin desviarse, porque igual que en caso de la reja, la mayor parte del espacio de un átomo es espacio vacío.
|
 |
Algunas se desviaban, porque pasan muy cerca de centros con carga eléctrica del mismo tipo que las partículas alfa (CARGA POSITIVA).
|
 |
Muy pocos rebotaban, porque chocan frontalmente contra esos centros de carga positiva.
|
El modelo del átomo de Rutherford se parecía a un sistema solar en miniatura, con los protones en el núcleo y los electrones girando alrededor.
|
A continuación tienes un applet en el que se simula el experimento de rutherford.
El applet anterior pertenece al curso de Física de Ángel Franco cuya dirección es
http://www.sc.ehu.es/sbweb/fisica/default.htm
http://www.sc.ehu.es/sbweb/fisica/default.htm
EL NÚCLEO ATÓMICO
Es una pequeña región central del átomo donde se encuentran distribuidos los neutrones y protones, partículas fundamentales del núcleo, que reciben el nombre de nucleones.
 | La estabilidad del núcleo no puede explicarse por su acción eléctrica. Al contrario, la repulsión existente entre los protones produciría su desintegración. El hecho de que en el núcleo existan protones y neutrones es un indicador de que debe existir otra interacción más fuerte que la electromagnética que no está directamente relacionada con cargas eléctricas y que es mucho más intensa. Esta interacción se llama interacción nuclear fuerte y es la que predomina en el núcleo. |
Para explicar la naturaleza de las fuerzas nucleares que mantienen unidas a las partículas dentro de los núcleos, es necesario analizar sus propiedades. En general, un núcleo tiene masa y está cargado eléctricamente. Además, tiene un tamaño que se puede medir por su radio. Los nucleones se mueven bajo la acción de sus interacciones mutuas y la intensidad de sus interacciones se puede medir por su energía de enlace o energía de ligadura nuclear.
A) NÚMERO MÁSICO. CLASIFICACIÓN DE LOS NUCLEIDOS O NÚCLIDOS
Igual que todos los átomos que tienen el mismo número atómico, pertenecen al mismo elemento químico, todos los núcleos que tienen igual número de protones e igual número de neutrones, pertenecen al mismo nucleido o núclido.
Un núcleo está constituido por un número de neutrones y un número de protones cuya suma recibe el nombre de número másico y se representa por A.
A = N + Z
Notación: AzX
A = número másico
N = número de neutrones
Z = número de protones
Los distintos núclidos del mismo elemento químico se llaman isótopos.
· Isótopos: son núcleos con igual número de protones, pero distinto número de neutrones, y por tanto distinto número másico.
Para referirse a un determinado isótopo, se escribe así: AZX. Aquí X es el símbolo químico del elemento, Z es el número atómico, y A es el número de neutrones + protones, llamado número másico. Por ejemplo, el hidrógeno ordinario se escribe 11H, el deuterio es 21H, y el tritio es 31H.
| protio (es un protón) 11H | deuterio 21H | tritio 31H |
 |  |  |
ESTABILIDAD NUCLEAR
Un núcleo se considera estable si no se transmuta espontáneamente en 1021años, si bien puede transmutarse en otros núcleos bajo ciertas condiciones.
Hay 115 elementos químicos conocidos, de los cuales, 92 existen en la naturaleza y el resto han sido obtenido artificialmente. Se conocen hoy en día unos 2000 núclidos, de los cuales son estables 274. Unos 340 existen en la Naturaleza y el resto se han producido en el laboratorio. Por tanto, la mayoría de los núclidos son radiactivos.
Los núclidos radiactivos son inestables y se transforman espontáneamente con el tiempo formando otros núclidos.
Los núclidos radiactivos son inestables y se transforman espontáneamente con el tiempo formando otros núclidos.
B) CARGA Y TAMAÑO DEL NÚCLEO
La carga del núcleo determina su posición en el sistema periódico. Rutherford demostró que la mayor parte de la masa del átomo y su carga positiva están localizados en una pequeña región central del átomo que llamó núcleo, cuyo radio estimó del orden de 10-14m a través del estudio de dispersión de partículas alfa al incidir en núcleos de átomos metálicos.
El radio nuclear ha sido calculado posteriormente, siendo del orden de 10-15m., y resultando ser proporcional al número másico A:
R = ro.A1/3
roes un valor constante para todos los núcleos y es igual a 1'3.10-15m.
Por tanto, el volumen de un núcleo si se considera su forma esférica, es proporcional al número A de nucleones, y la densidad nuclear es un valor constante, 1015 veces mayor que la densidad de la materia macroscópica, lo que da una idea de la gran compacidad de los nucleones dentro de un núcleo. Así mismo, demuestra que la materia macroscópica está esencialmente vacía, ya que la mayor parte de la masa está concentrada en los núcleos.
C) ENERGÍA DE ENLACE NUCLEAR
Se define como la energía necesaria para separar los nucleones de un núcleo, o bien como la energía que se libera cuando se unen los nucleones para formar el núcleo.
El origen de la energía de ligadura o de enlace nuclear reside en la desaparición de una parte de la masa de los nucleones que se combinan para formar el núcleo. Esta diferencia de masa recibe el nombre de defecto másico Dm, y se transforma en energía cuyo cálculo se puede realizar por la ecuación de Einstein, E=m c2
Si a la suma de las masas de los nucleones y electrones de un átomo le restamos la masa medida experimentalmente a través del espectrógrafo de masas, obtenemos el defecto másico, y podemos calcular la energía total de enlace. La energía de enlace o de ligadura será equivalente a la energía liberada en la formación de un núcleo.
La u.m.a. se define como la doceava parte de la masa del átomo 612C y 1 u.m.a.=1'66.10-27Kg, sustituyendo en la ecuación de Einstein, E=m c2,se obtiene E = 931 MeV, es decir, 1 u.m.a. libera 931 MeV. Por tanto, la energía liberada (Ee) en la formación de un núcleo será:
Ee = Dm × 931 MeV.
Ee = Dm × 931 MeV.
Ahora bien, es más interesante calcular la energía de enlace por nucleón (Ee/A) y representarla frente al número másico A. La energía de enlace por nucleón se obtiene dividiendo la energía de enlace del núcleo por sus A nucleones.

Si bien en los núcleos livianos se observa un aumento abrupto de la energía de enlace por nucleón frente al número másico A, a partir de A=10, la energía de enlace por nucleón es prácticamente constante.
El máximo corresponde a núcleos semipesados con A=62 (Fe, Co, Ni), donde las fuerzas de atracción serán máximas. El decrecimiento de la energía para A>60 se debe a la repulsión eléctrica entre los protones cuyo número va aumentando y reduce por tanto la estabilidad de los núcleos. En los núcleos ligeros, cada nucleón es atraído por pocos nucleones, lo que también reduce su estabilidad.
D) CARACTERÍSTICAS DE LAS FUERZAS NUCLEARES
· Las fuerzas nucleares son fuerzas atractivas de gran intensidad dado el tamaño de los núcleos y su enorme densidad, que predominan en el núcleo venciendo la repulsión electrostática entre los protones.
· Son de corto alcance, es decir, cada nucleón interacciona con los nucleones más próximos, si bien a distancias muy cortas, las fuerzas nucleares se hacen repulsivas lo que explica que los nucleones permanezcan a distancias medias constantes y que el volumen por nucleón sea constante.
· La fuerza de interacción entre dos nucleones es independiente de la carga, por lo que la fuerza entre dos nucleones, bien sean protón-protón, neutrón-neutrón o protón-neutrón, es aproximadamente la misma.
3. radioactividad
Definimos radioactividad como la emisión espontánea de partículas (alfa, beta, neutrón) o radiaciones (gama, captura K), o de ambas a la vez, procedentes de la desintegración de determinados nucleidos que las forman, por causa de un arreglo en su estructura interna.
La radioactividad puede ser natural o artificial. En la radioactividad natural, la sustancia ya la posee en el estado natural. En la radioactividad artificial, la radioactividad le ha sido inducida por irradiación.
Un radionucleido es el conjunto de los núcleos radioactivos de una misma especie. Todos los núcleos radioactivos que forman un radionucleido tienen una radiactividad bien definida, común a todos ellos, que los identifica; de la misma forma que un tipo de reacción química identifica los elementos que participan.
Cuantitativamente, la radioactividad es un fenómeno estadístico. Por este motivo, para valorarlo hay que observar el comportamiento de un conjunto de núcleos de la misma especie. Por la ley de los grandes números, se define una constante radiactiva λ como la probabilidad de desintegración de un núcleo por unidad de tiempo. Con esta definición, el número N de núcleos radioactivos de una misma especie que se encuentran en una sustancia en un instante t es dado por N = No · e-λt, donde No es el número de núcleos radioactivos que había antes de que transcurriera el tiempo t. En realidad, difícilmente una sustancia radioactiva es formada por un solo radionucleido, aunque cada uno de sus componentes en desintegrarse se transforma en un núcleo diferente que, a su vez, puede ser también radioactivo.
El radionucleido inicial es llamado padre, y el derivado, hijo. Esta situación puede continuar a lo largo de múltiples filiaciones y el conjunto de todas es llamado familia o serie radioactiva. En este caso, la relación que da el número de núcleos radioactivos presentes es más compleja porque, además de tener en cuenta el número de cada uno de ellos en el instante inicial, hay que considerar que, por desintegración de unos, se forman otros.
El problema se simplifica cuando se quiere conseguir el equilibrio radioactivo (dicho también equilibrio secular en las series radiactivas naturales), que es cuando ha pasado un tiempo suficientemente largo desde que se ha iniciado el proceso de filiación, porque entonces el ritmo de las desintegraciones es impuesto por el radionucleido que tiene la constante radioactiva más pequeña.
Nucleidos radioactivos naturales
En la naturaleza se encuentran unos 300 nucleidos diferentes, de los cuales 25 son radioactivos con un período suficientemente largo para que haya aún hoy en día; otros 35 tienen un período mucho más corto y se crean y se desintegran continuamente en las series radiactivas.
Nucleidos radioactivos artificiales
Han sido creados e identificados más de 1000 radionucleidos artificiales. Las series radioactivas reciben el nombre del nucleido padre de períodos más largo. Hay cuatro. Tres de estas series radioactivas son naturales: la del torio, la del uranio y la del actinio, que terminan en sus propios isótopos estables del plomo. Estos isótopos tienen respectivamente los números de masa 208, 206 y 207. Respecto a la serie del neptunio, como los radionucleidos que la componen tienen un período corto comparado con la duración de las eras geológicas, no se encuentra en la naturaleza y ha sido obtenida artificialmente. El último nucleido de esta serie es el isótopo 209 del bismuto.
Origen de la radioactividad
La radioactividad fue descubierta en 1896 por Antonie-Henri Becquerel, el cual, al hacer estudios sobre la fosforescencia de las sustancias, observó que un mineral de uranio era capaz de velar unas placas fotográficas que eran guardadas a su lado.
4 Fusión y fisión nuclear |
FISIÓN:
Como se puede comprobar, en cada reacción sucesiva, se rompen 3n átomos, donde n indica 1ª, 2ª, 3ª,..., reacción.

Otra reacción nuclear de fisión que ocurre en muchos reactores nucleares es:
El Uranio natural es mayoritariamente U-238, el que es fisionable es el U-235, que es un 0.71% del Uranio que se encuentra en la naturaleza, de ahí que solo un pequeño porcentaje del Uranio se aproveche y se requieran grandes cantidades de este para obtener una cantidad significativa de U-235.
Las barras con el U-235 se introducen en el reactor, y comienza un proceso de fisión. En el proceso, se desprende energía en forma de calor. Este calor, calienta unas tuberías de agua, y esta se convierte en vapor, que pasa por unas turbinas, haciéndolas girar. Estas a su vez, hacen girar un generador eléctrico, produciendo así electricidad. Lógicamente, no se aprovecha toda la energía obtenida en la fisión, parte de ella se pierde en calor, resistencia de los conductores, vaporización de agua, etc.
Los neutrones son controlados para que no explote el reactor mediante unas barras de control (generalmente, de Carburo de Boro), que al introducirse, absorben neutrones, y disminuye el número de fisiones, con lo cual, dependiendo de cuántas barras de control se introduzcan, se generará más o menos energía. Normalmente, se introducen las barras de tal forma, que solo se produzca un neutrón por reacción de fisión, controlando de esta forma el proceso de fisión. Si todas las barras de control son introducidas, se absorben todos los neutrones, con lo cual se pararía el reactor.
El reactor se refrigera, para que no se caliente demasiado, y funda las protecciones, incluso cuando este esté parado, ya que la radiación hace que el reactor permanezca caliente.


FUSIÓN:
La fusión nuclear, está actualmente en líneas de investigación, debido a que todavía hoy no es un proceso viable, ya que se invierte más energía en el proceso para que se produzca la fusión, que la energía obtenida mediante este método.
La fusión, es un proceso natural en las estrellas, produciéndose reacciones nucleares por fusión debido a su elevadísima temperatura interior.
Las estrellas están compuestas principalmente por Hidrógeno y Helio. El hidrógeno, en condiciones normales de temperatura, se repele entre sí cuando intentas unirlo (fusionarlo) a otro átomo de hidrógeno, debido a su repulsión electrostática. Para vencer esta repulsión electrostática, el átomo de hidrógeno debe chocar violentamente contra otro átomo de hidrógeno, fusionándose, y dando lugar a Helio, que no es fusionable. La diferencia de masa entre productos y reactivos es mayor que en la fisión, liberándose así una gran cantidad de energía (muchísimo mayor que en la fisión). Estos choques violentos, se consiguen con una elevada temperatura, que hace aumentar la velocidad de los átomos.
La primera reacción de fusión artificial, tuvo origen en la investigación militar, fue una bomba termonuclear (o también llamada bomba-H o de Hidrógeno), para obtener la temperatura adecuada que inicia el proceso de fusión (unos 20 millones de grados centígrados) se utilizó una bomba atómica.
Ejemplos característicos de reacciones de fusión son los siguientes: